弱酸性次亜塩素酸についてSTERILIXATION・DEODORANT
殺菌の主役は次亜塩素酸!
次亜塩素酸(HClO)はオゾンや二酸化塩素と同様に酸化分解により菌やウィルスを破壊します。
だから、アルコールのように耐性菌はできません。
しかも、オゾンや二酸化塩素のように毒性がなく、人に優しい殺菌剤なのです。
次亜塩素酸は、医薬品や食品添加物指定の殺菌剤である次亜塩素酸ソーダ(ナトリウム)に僅かに含まれています。だから次亜塩素酸ソーダには殺菌力があるのです。
でも、通常次亜塩素酸ソーダはアルカリ性で、一般的に使われる200ppm(ppmとは1/1,000,000と言う単位)の濃度ではpH8〜9程度です。
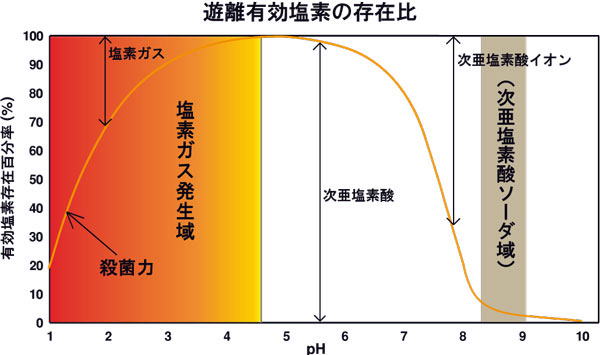
この時、下のグラフから見て分るように次亜塩素酸は10%程度しか含まれていません。
ここで、pHとは7が中性で、数字が小さくなると酸性、大きくなるとアルカリ性です。グラフから見ると、pHが5くらいの弱酸性で最も次亜塩素酸(HClO)の比率が高くなり、ほぼ100%に達しています。そして、pH5よりも小さくなると、次亜塩素酸が減って塩素ガス(Cl:人体に有害なガス)が発生してきています。
つまり、次亜塩素酸の比率が高く塩素ガスの出ない領域(pH5〜6.5)で使うのが最も殺菌効率が良くなります。ただ、pH5よりも下がると塩素ガスがでるため、安全を考慮してpH5.5〜6.5で使用するのが良いでしょう。
だから、アルコールのように耐性菌はできません。
しかも、オゾンや二酸化塩素のように毒性がなく、人に優しい殺菌剤なのです。
次亜塩素酸は、医薬品や食品添加物指定の殺菌剤である次亜塩素酸ソーダ(ナトリウム)に僅かに含まれています。だから次亜塩素酸ソーダには殺菌力があるのです。
でも、通常次亜塩素酸ソーダはアルカリ性で、一般的に使われる200ppm(ppmとは1/1,000,000と言う単位)の濃度ではpH8〜9程度です。
この時、下のグラフから見て分るように次亜塩素酸は10%程度しか含まれていません。
ここで、pHとは7が中性で、数字が小さくなると酸性、大きくなるとアルカリ性です。グラフから見ると、pHが5くらいの弱酸性で最も次亜塩素酸(HClO)の比率が高くなり、ほぼ100%に達しています。そして、pH5よりも小さくなると、次亜塩素酸が減って塩素ガス(Cl:人体に有害なガス)が発生してきています。
つまり、次亜塩素酸の比率が高く塩素ガスの出ない領域(pH5〜6.5)で使うのが最も殺菌効率が良くなります。ただ、pH5よりも下がると塩素ガスがでるため、安全を考慮してpH5.5〜6.5で使用するのが良いでしょう。
下の表は、pH5.2で塩素濃度57ppmの次亜塩素酸と、pH9で塩素濃度200ppmの次亜塩素酸ソーダの殺菌効果試験データです。
大腸菌や黄色ブドウ球菌等の弱い菌では差が出ませんが、枯草菌(芽胞菌)やカビ類では大きな差が見られます。
これが、次亜塩素酸の殺菌力(即効性)の証です。
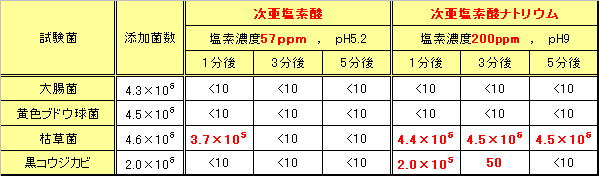
※<10は検出不能を意味します。 試験温度23℃ (財)日本食品分析センター
また、下のデータは、同じpH5.2で塩素濃度を80ppmに上げた次亜塩素酸による殺菌効果試験データです。
全ての菌が1分後には検出されなくなっています。
このように、次亜塩素酸は、ほぼ全ての菌やウィルスの殺菌ができます。
※ただし、これらのデータは試験管データで、実際には次亜塩素酸は他の有機物とも反応して消化されます。したがって、実際の使用においては、もう少し濃度を上げるか濃度が落ちないように常に新しい次亜塩素酸を追加することが重要です。
全ての菌が1分後には検出されなくなっています。
このように、次亜塩素酸は、ほぼ全ての菌やウィルスの殺菌ができます。
※ただし、これらのデータは試験管データで、実際には次亜塩素酸は他の有機物とも反応して消化されます。したがって、実際の使用においては、もう少し濃度を上げるか濃度が落ちないように常に新しい次亜塩素酸を追加することが重要です。
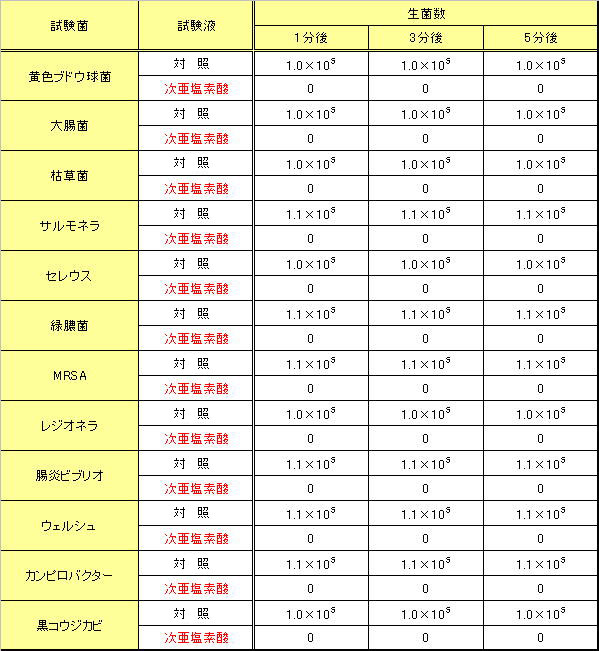 試験温度23℃
試験温度23℃さらに、次亜塩素酸を空間に噴霧することにより、浮遊菌の殺菌もできます。
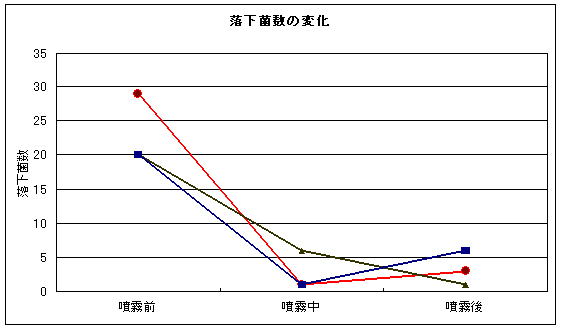
下のグラフは、6床の病室に次亜塩素酸(200ppm)を1時間噴霧した時の落下菌の変化示すグラフです。噴霧中のデータは噴霧開始から30分後のデータです。病室への看護士の出入りは通常通りありました。
噴霧から30分以内で激減し、その後殆ど変わっていません。また、噴霧前に陽性だったMRSAも噴霧中間(30分後)以降は陰性となりました。
下のグラフは、6床の病室に次亜塩素酸(200ppm)を1時間噴霧した時の落下菌の変化示すグラフです。噴霧中のデータは噴霧開始から30分後のデータです。病室への看護士の出入りは通常通りありました。
噴霧から30分以内で激減し、その後殆ど変わっていません。また、噴霧前に陽性だったMRSAも噴霧中間(30分後)以降は陰性となりました。
消臭にも次亜塩素酸
次亜塩素酸は、特に有機物の消臭に効果があり、下のグラフのように強い消臭力があります。また、臭いの元は菌であることが多く、殺菌することにより臭いの元を断ち、完全に消臭することができます。
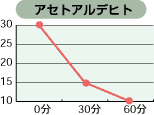
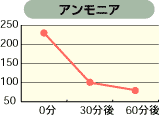
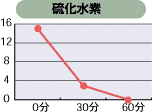
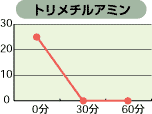
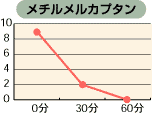
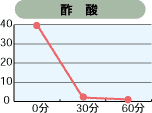 塩素濃度:80ppmにてテスト
塩素濃度:80ppmにてテスト
従来の消臭剤は臭いを除去する働きよりも香りで悪臭を抑える物が多くありました。次亜塩素酸は化学反応により悪臭を無臭の成分に変化させるため臭いが残りません。
特に、悪臭の4大要素であるアンモニアについては次のような反応により無臭になります。
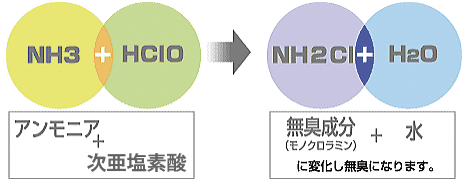
※クロラミンは有機物などとの反応がゆっくりと進行するので、残留効果があり、臭いを発するような成分を生成しない利点があって1920〜1930年代にヨーロッパの一部やわが国でも使用された殺菌方法です。
動物病院では、専用の超音波噴霧器を使用して、臭いが気になる待合室・オペ室・犬舎で噴霧しています。また、ペットの排出物の消臭にも効果的です。
特に、悪臭の4大要素であるアンモニアについては次のような反応により無臭になります。


※クロラミンは有機物などとの反応がゆっくりと進行するので、残留効果があり、臭いを発するような成分を生成しない利点があって1920〜1930年代にヨーロッパの一部やわが国でも使用された殺菌方法です。
動物病院では、専用の超音波噴霧器を使用して、臭いが気になる待合室・オペ室・犬舎で噴霧しています。また、ペットの排出物の消臭にも効果的です。
次亜塩素酸の安全性
次亜塩素酸は、人間が外部から進入した菌やウィルスを退治する際に血液中で作り出す成分です。つまり、次亜塩素酸は人間にとって馴染みの深い物質なのです。
50ppmの次亜塩素酸で動物安全性試験を行った結果です。
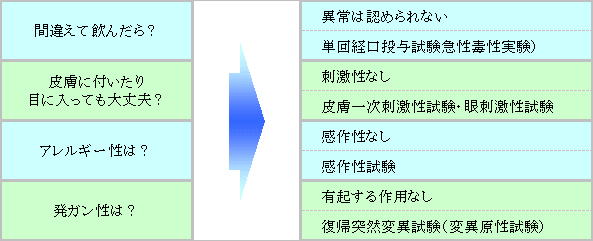
50ppmの次亜塩素酸で動物安全性試験を行った結果です。

次亜塩素酸の歴史
古くから次亜塩素酸(HClO)の殺菌力が高い(即効性がある)ことは知られていました。
次亜塩素酸は、以下の3つの特徴があり、殺菌には最適です。
1.殺菌力が強く低濃度および短時間で殺菌できる。
2.残留性が低く、簡単に洗い流せる。
3.トリハロメタンができない。
次亜塩素酸ソーダ(NaClO)は、次亜塩素酸(HClO)と次亜塩素酸イオン(ClO+)に解離しており、90%が次亜塩素酸イオンです(上のグラフでは、殺菌力曲線の上側の部分)。次亜塩素酸イオンには殺菌力が殆ど無く、次亜塩素酸により殺菌が進み次亜塩素酸が消化されると、約1:9の比率を保つように次亜塩素酸イオンが次亜塩素酸に変化します。つまり、ゆっくりと殺菌が進みます。したがって、次亜塩素酸イオンがいつまでも残り残留性を高くしてしまいます。
それに比べて、弱酸性の次亜塩素酸ソーダには、次亜塩素酸イオンは10%程度しか含まれておらず、ほぼ全てが殺菌成分の次亜塩素酸です。したがって、殺菌速度が速く次亜塩素酸イオンの残留も少ないのです。
そして、次亜塩素酸ソーダの問題でもあるトリハロメタンですが、このトリハロメタンはアルカリ性領域で生成されますが、酸性領域では生成されないのです。
こんな便利な次亜塩素酸が何故普及しなかったのかと言うと、理由が2つあります。
1.作るのが非常に難しい(安定しない、高い)
2.保存性が無い
つまり、簡単に作ることができなかったのと、せっかく作っても長期保存ができないので非常に不便だったのです。
次亜塩素酸を作る方法として最初に現れたのが電気分解方式です。
この方法にも以下のように更に3つの方法があります。
1.食塩水を電気分解して、陰極でできたアルカリ水と陽極でできた強酸性水を混ぜて弱酸性の次亜塩素酸を作る方法
2.食塩水に塩酸を混ぜた物を電気分解して直接弱酸性の次亜塩素酸を作る方法
3.塩酸だけを混ぜた水を電気分解して直接弱酸性の次亜塩素酸を作る方法
それぞれ、特徴はありますが、何れも高価な電極(白金とチタン)を使用し、電極が消耗品のため維持費が掛かります。
次に出てきたのが、次亜塩素酸に塩酸を混ぜて、無理やり弱酸性にする方法です。
この方法は、構造が簡単で消耗品も無く安く大量に次亜塩素酸を作ることができます。
しかし、致命的は欠点がありました。
次亜塩素酸ソーダは「塩素系殺菌剤」、塩酸は勿論「酸」です。塩素系の漂白剤などで、「混ぜるな危険」の文字を見たことがあると思いますが、この混ぜると塩素ガスが出る2つの薬剤を混ぜているのです。
また、次亜塩素酸ソーダに塩酸を混ぜると、pH7くらいから急激にpHが下がり一気にpH3以下の強酸性になってしまいます。このpH3という領域は、大量に塩素ガスが出る領域です。
したがって、装置の制御が非常に難しく、さらに、人的ミスによっても塩素ガスが発生する危険な方法です。
ヴィータが開発した方法は、次亜塩素酸ソーダに炭酸ガスを混合して弱酸性の次亜塩素酸を作る方法です。
炭酸ガスは、pH緩衝性(pH値が変化しないように自己コントロールする性質)を持っており、間違ってもpH5以下になることはありません。しかも、次亜塩素酸ソーダに少し炭酸ガスを加えるだけでpHが6.5以下に下がり、どんなに加えても5以下には下がりません。
この、塩酸と炭酸ガスのpH変化を図示した物が下のグラフです。
次亜塩素酸は、以下の3つの特徴があり、殺菌には最適です。
1.殺菌力が強く低濃度および短時間で殺菌できる。
2.残留性が低く、簡単に洗い流せる。
3.トリハロメタンができない。
次亜塩素酸ソーダ(NaClO)は、次亜塩素酸(HClO)と次亜塩素酸イオン(ClO+)に解離しており、90%が次亜塩素酸イオンです(上のグラフでは、殺菌力曲線の上側の部分)。次亜塩素酸イオンには殺菌力が殆ど無く、次亜塩素酸により殺菌が進み次亜塩素酸が消化されると、約1:9の比率を保つように次亜塩素酸イオンが次亜塩素酸に変化します。つまり、ゆっくりと殺菌が進みます。したがって、次亜塩素酸イオンがいつまでも残り残留性を高くしてしまいます。
それに比べて、弱酸性の次亜塩素酸ソーダには、次亜塩素酸イオンは10%程度しか含まれておらず、ほぼ全てが殺菌成分の次亜塩素酸です。したがって、殺菌速度が速く次亜塩素酸イオンの残留も少ないのです。
そして、次亜塩素酸ソーダの問題でもあるトリハロメタンですが、このトリハロメタンはアルカリ性領域で生成されますが、酸性領域では生成されないのです。
こんな便利な次亜塩素酸が何故普及しなかったのかと言うと、理由が2つあります。
1.作るのが非常に難しい(安定しない、高い)
2.保存性が無い
つまり、簡単に作ることができなかったのと、せっかく作っても長期保存ができないので非常に不便だったのです。
次亜塩素酸を作る方法として最初に現れたのが電気分解方式です。
この方法にも以下のように更に3つの方法があります。
1.食塩水を電気分解して、陰極でできたアルカリ水と陽極でできた強酸性水を混ぜて弱酸性の次亜塩素酸を作る方法
2.食塩水に塩酸を混ぜた物を電気分解して直接弱酸性の次亜塩素酸を作る方法
3.塩酸だけを混ぜた水を電気分解して直接弱酸性の次亜塩素酸を作る方法
それぞれ、特徴はありますが、何れも高価な電極(白金とチタン)を使用し、電極が消耗品のため維持費が掛かります。
次に出てきたのが、次亜塩素酸に塩酸を混ぜて、無理やり弱酸性にする方法です。
この方法は、構造が簡単で消耗品も無く安く大量に次亜塩素酸を作ることができます。
しかし、致命的は欠点がありました。
次亜塩素酸ソーダは「塩素系殺菌剤」、塩酸は勿論「酸」です。塩素系の漂白剤などで、「混ぜるな危険」の文字を見たことがあると思いますが、この混ぜると塩素ガスが出る2つの薬剤を混ぜているのです。
また、次亜塩素酸ソーダに塩酸を混ぜると、pH7くらいから急激にpHが下がり一気にpH3以下の強酸性になってしまいます。このpH3という領域は、大量に塩素ガスが出る領域です。
したがって、装置の制御が非常に難しく、さらに、人的ミスによっても塩素ガスが発生する危険な方法です。
ヴィータが開発した方法は、次亜塩素酸ソーダに炭酸ガスを混合して弱酸性の次亜塩素酸を作る方法です。
炭酸ガスは、pH緩衝性(pH値が変化しないように自己コントロールする性質)を持っており、間違ってもpH5以下になることはありません。しかも、次亜塩素酸ソーダに少し炭酸ガスを加えるだけでpHが6.5以下に下がり、どんなに加えても5以下には下がりません。
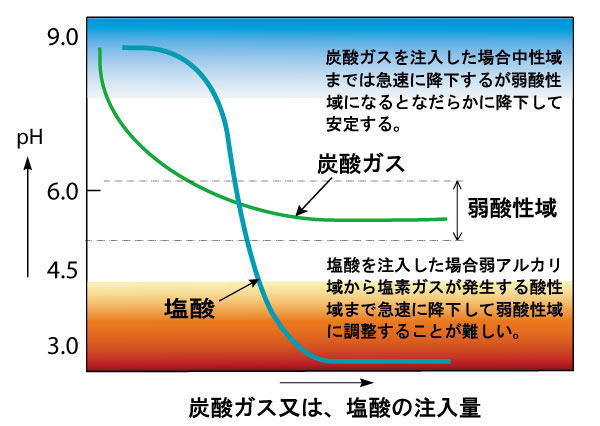
この、塩酸と炭酸ガスのpH変化を図示した物が下のグラフです。
図の説明
上のグラフは、次亜塩素酸ソーダに少しずつ塩酸または炭酸ガスを加えたときのpH変化を表したグラフです。塩酸を加えて行くと、ゆっくりとpHが下がりpH7くらいから急激にpHが下がりpH3以下にまで落ちます。炭酸ガスの場合は、少し加えただけでpHが下がり、その後は加えすぎてもpH5くらいで止まります。
つまり、炭酸ガスの場合は、最適なpH5.5〜6.5に安定的に維持できる優れものなのです。
ただ、唯一の欠点は、時間がつと炭酸ガスが抜けて行きpHが徐々に上ってくることです。したがって、作ったら2〜3日で使い切って頂くことをお奨めしています。
ヴィータ株式会社
〒356-0005
埼玉県ふじみ野市西2-7-18
【お問合せ先】
ヴィータ販売株式会社
■本社(埼玉県ふじみ野市)
TEL 049-265-8901
FAX 049-256-2382
info@veeta.co.jp
■大阪営業所(大阪府茨木市)
TEL 072-658-6930
FAX 072-655-3456


